Modell der Multiplen Sklerose
Multiple Sklerose ist eine Autoimmunerkrankung des zentralen Nervensystems (ZNS), die durch eine entzündliche Demyelinisierung gekennzeichnet ist. Häufig geht die Krankheit mit einer Entzündung des Sehnervs einher, die zu einer Sehbehinderung führen kann (Shindler et al. 2012). Diese Sehstörungen sind oft frühe Symptome der Multiplen Sklerose.
In früheren Studien wurden der Sehnerv und die Netzhautstrukturen in einem experimentellen Autoimmunenzephalomyelitismodell (EAE; Horstmann et al. 2013) analysiert. Wir konnten eine starke Korrelation zwischen dem Grad der Immunzellinfiltration bzw. dem Demyelinisierungswert und den klinischen Symptomen nachweisen. Sobald der Sehnerv degenerierte, war auch die Netzhaut betroffen. Daher wurde die Netzhaut analysiert. Untersuchungen der Netzhaut zeigten deutlich mehr apoptotische retinale Ganglienzellen (RGC) sowie einen RGC-Verlust bei EAE-Tieren (Abbildung 1). Es wurden also strukturelle Veränderungen der Netzhaut beobachtet. Multiple Sklerose wird auch mit Autoimmunmechanismen in Verbindung gebracht (Hendrickx et al. 2014). Daher wurden Mikroglia und Makrophagen in dem EAE-Modell untersucht. Es wurde ein Anstieg sowohl der Mikroglia- als auch der Makrophagenpopulation gemessen, sowie eine erhöhte Interleukin-6-Produktion (Horstmann et al., 2013). Diese Mechanismen sind charakteristisch für Entzündungsprozesse. In einem nächsten Schritt sollte die mögliche Wirkung bestimmter Therapeutika auf retinale Strukturen und Immunzellinfiltrate analysiert werden.
Abbildung 1: Ganglienzelluntergang

A) Die Zellen der Flatmounts wurden mit einem unspezifischen Nissel-Farbstoff markiert. B) Es wurde eine signifikante Abnahme der RGCs festgestellt (p<0,001). C) RGCs wurden mit einem spezifischen Marker, Brn-3a (rot), auf Querschnitten der Netzhaut sichtbar gemacht (weiße Pfeile). D) Auch mit dem spezifischen Marker wurde ein Zellverlust festgestellt (p=0,02). Maßstabsleiste: 25 µm. Die Daten sind Mittelwerte ± SEM. *: p<0,05; ***: p<0,001. Abkürzungen: CO=Kontrolle, EAE=behandelt; GCL=Ganglienzellschicht, IPL=innere plexiforme Schicht, INL=innere Kernschicht (modifiziert nach Horstmann et al., 2013).
Experimentelles Modell für Neuromyelitis-optica-Spektrum Störungen
Erkrankungen des ZNS haben aufgrund der möglichen Entwicklung von Behinderungen tiefgreifende Folgen für die Patienten. Während MS die häufigste Ursache ist, gibt es auch ein Spektrum von relativ seltenen neuroinflammatorischen und neurodegenerativen Erkrankungen, darunter Neuromyelitis-optica-Spektrum-Erkrankungen (NMOSD). Insgesamt 25% der Patienten mit einem NMOSD-Phänotyp weisen Autoantikörper auf, die gegen das Myelin-Oligodendrozyten-Glykoprotein (MOG; Delarasse et al. 2003) gerichtet sind. Um die Pathogenese der Krankheit besser zu verstehen, nutzten wir ein Tiermodell der spontanen optikospinalen Enzephalomyelitis (OSE). OSE-Mäuse entwickeln spontan eine progressive Enzephalomyelitis, die durch Entzündung und Demyelinisierung des Rückenmarks und des Sehnervs gekennzeichnet ist (Optic Neuritis Study 2008; Krishnamoorthy et al. 20106).
In unsere Studie haben wir bereits die longitudinale Dynamik morphologischer, funktioneller und struktureller Netzhautveränderungen sowie (immun-)histochemischer Veränderungen des Sehnervs bei OSE-Mäusen untersucht. Wir konnten zeigen, dass OSE-Mäuse am Tag 38 klinische Anzeichen einer Enzephalomyelitis mit einer Inzidenz von 75 % aufwiesen. Anschließend untersuchten wir die Anzahl der RGCs in 6 und 8 Wochen alten Mäusen. Nach 6 Wochen war die Anzahl der RGCs bei OSE-Mäusen im Vergleich zur Kontrollgruppe um 37,8 % reduziert. Bei 8 Wochen alten OSE-Mäusen wurde ein Rückgang der RGCs um 27,4 % festgestellt (Abbildung 2A-C). Entsprechend waren die mRNA-Expressionsniveaus des RGC-Markers Pou4f1 sowohl in der 6 Wochen alten als auch in der 8 Wochen alten OSE-Maus signifikant herabreguliert.
Abbildung 2: Retinaler Ganglienzellverlust bei OSE-Mäusen
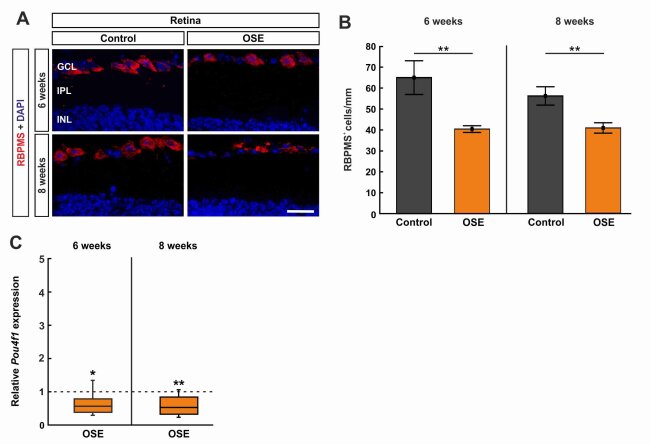
A) Retinale Ganglienzellen wurden mit RBPMS (rot) auf Netzhautquerschnitten angefärbt. Die Zellkerne wurden mit DAPI (blau) gefärbt. B) Die Anzahl der RGC war in der OSE-Gruppe nach sechs und acht Wochen signifikant reduziert. C) Bei OSE-Mäusen wurde nach sechs und acht Wochen eine signifikante Downregulation der Pou4f1-mRNA festgestellt. Maßstabsbalken: 20 µm. Daten sind Mittelwerte ± SEM für die Immunhistochemie, relative Werte für RT-qPCR sind Median ± Quartil ± Maximum/Minimum. Die gepunktete Linie in C stellt das relative Expressionsniveau der Kontrollgruppe dar. *p < 0,05, **p < 0,01. Abkürzungen: GCL=Ganglienzellschicht; IPL=innere plexiforme Schicht; INL=innere Kernschicht. (Petrikowski et al., 2022)