Faculty of Chemistry
and Biochemistry
Biochemistry II
Biomolecular NMR Spectroscopy
Prof. Dr. Raphael Stoll
Building NC 5/171
Universitätsstraße 150
D-44780 Bochum
Tel.: +49 234 32-25466
Fax: +49 234 32-05466
E-Mail: bionmr@rub.de
News
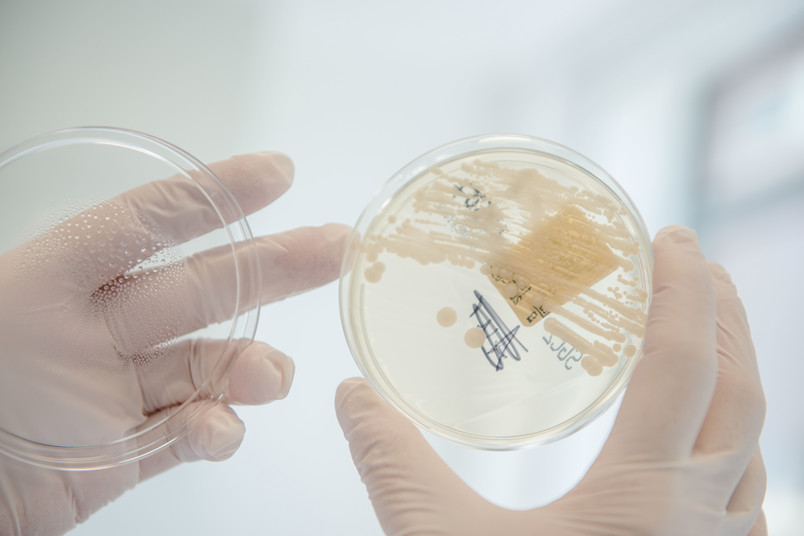 Twenty years ago, a drug candidate was rejected due to its side effects. Researchers have now figured out how to potentially make a successor molecule more selective. An increasing number of bacteria have become resistant to many commonly used antibiotics. Researchers from Bochum have discovered a fresh opportunity for a potential active molecule whose predecessor was rejected: By studying its interaction with the bacterial target protein very precisely in three dimensions, they identified a previously undetected point of attack that could be targeted by this compound. “As this point of attack only occurs in bacterial proteins, the drug would become much more selective and its harmfulness to human cells would be reduced,” explains Professor Raphael Stoll, head of the Biomolecular NMR Spectroscopy research group at the Faculty of Chemistry and Biochemistry at Ruhr University Bochum, Germany. The researchers published their findings on April 4, 2024 in the Journal of Medicinal Chemistry.
Twenty years ago, a drug candidate was rejected due to its side effects. Researchers have now figured out how to potentially make a successor molecule more selective. An increasing number of bacteria have become resistant to many commonly used antibiotics. Researchers from Bochum have discovered a fresh opportunity for a potential active molecule whose predecessor was rejected: By studying its interaction with the bacterial target protein very precisely in three dimensions, they identified a previously undetected point of attack that could be targeted by this compound. “As this point of attack only occurs in bacterial proteins, the drug would become much more selective and its harmfulness to human cells would be reduced,” explains Professor Raphael Stoll, head of the Biomolecular NMR Spectroscopy research group at the Faculty of Chemistry and Biochemistry at Ruhr University Bochum, Germany. The researchers published their findings on April 4, 2024 in the Journal of Medicinal Chemistry.
 Discovery of the MOTH domain offers insights into evolution. This is because both insects and vertebrates need collagen in their connective tissue.
Collagen is the protein that holds our body together. It is produced inside cells, from where it must be transported to its site of action in connective tissue. The protein domain that is responsible for the recognition of collagen has previously been mistaken for a subform of another. Dr. Oliver Arnolds and Professor Raphael Stoll from the Faculty of Chemistry and Biochemistry at Ruhr University Bochum, Germany, have characterised and named this domain for the first time. They reported on the so-called MOTH domain of the TANGO1 protein family in the journal Nature Communications on 20 April 2023.
Discovery of the MOTH domain offers insights into evolution. This is because both insects and vertebrates need collagen in their connective tissue.
Collagen is the protein that holds our body together. It is produced inside cells, from where it must be transported to its site of action in connective tissue. The protein domain that is responsible for the recognition of collagen has previously been mistaken for a subform of another. Dr. Oliver Arnolds and Professor Raphael Stoll from the Faculty of Chemistry and Biochemistry at Ruhr University Bochum, Germany, have characterised and named this domain for the first time. They reported on the so-called MOTH domain of the TANGO1 protein family in the journal Nature Communications on 20 April 2023.
 While the correct function of many proteins depends on their three-dimensional structure, some appear to adopt random forms. For one of them, a team of researchers at Ruhr-Universität Bochum (RUB) has shown that the supposed disorder is not disorder after all: the protein HMGA1a adopts dynamic, more compact structures that depend on its phosphorylation. A malfunction of HMGA1a can lead to cancer. The researchers led by Profesoor Raphael Stoll therefore expect their results to form a basis for future therapeutic strategies to combat cancers caused by HMGA1a. They report in the journal Nucleic Acids Research on July, 24 2019.
While the correct function of many proteins depends on their three-dimensional structure, some appear to adopt random forms. For one of them, a team of researchers at Ruhr-Universität Bochum (RUB) has shown that the supposed disorder is not disorder after all: the protein HMGA1a adopts dynamic, more compact structures that depend on its phosphorylation. A malfunction of HMGA1a can lead to cancer. The researchers led by Profesoor Raphael Stoll therefore expect their results to form a basis for future therapeutic strategies to combat cancers caused by HMGA1a. They report in the journal Nucleic Acids Research on July, 24 2019.
Many – but not all – proteins in a living cell have a defined three-dimensional structure, which is absolutely necessary for their correct activity. The interrelationship between the structure and function of proteins is the focus of many research initiatives that extend to the development of innovative drugs.
Meeting with contributions from former students of Prof. W. Voelter
 K-Ras4B is a small GTPase that belongs to the Ras superfamily of guanine nucleotide-binding proteins. GTPases function as molecular switches in cells and are key players in intracellular signalling. Ras has been identified as an oncogene and is mutated in more than 20% of human cancers. Here, we report that Bisphenol S binds into a binding pocket of K-Ras4B previously identified for various low molecular weight compounds. Our results advocate for more comprehensive safety studies on the toxicity of Bisphenol S, as it is frequently used for Bisphenol A-free food containers..
K-Ras4B is a small GTPase that belongs to the Ras superfamily of guanine nucleotide-binding proteins. GTPases function as molecular switches in cells and are key players in intracellular signalling. Ras has been identified as an oncogene and is mutated in more than 20% of human cancers. Here, we report that Bisphenol S binds into a binding pocket of K-Ras4B previously identified for various low molecular weight compounds. Our results advocate for more comprehensive safety studies on the toxicity of Bisphenol S, as it is frequently used for Bisphenol A-free food containers..
 Viele Krankheiten wie etwa Krebs entstehen aus fehlerhaftem Verhalten von Proteinen. Wie sie interagieren und was dabei falsch ablaufen kann, können Forscher nun besser verstehen.
Viele Krankheiten wie etwa Krebs entstehen aus fehlerhaftem Verhalten von Proteinen. Wie sie interagieren und was dabei falsch ablaufen kann, können Forscher nun besser verstehen.
Seit 2004 fördert die Deutsche Forschungsgemeinschaft mit über 26 Millionen Euro den Sonderforschungsbereich 642 „GTP- und ATP-abhängige Membranprozesse“ (Sprecher: Prof. Dr. Klaus Gerwert). In 23 Teilprojekten untersuchten Bochumer und Dortmunder Wissenschaftler Signalwege und Transportprozesse innerhalb von Zellen, konnten sie räumlich und zeitlich auf verschiedenen Skalen auflösen und besser verstehen.
 Wir gratulieren recht herzlich unserer Mitarbeiterin Saskia Körning zum Wilke-Preis für den besten Zweifach-Bachelor-Abschluss 2015 in Chemie.
Wir gratulieren recht herzlich unserer Mitarbeiterin Saskia Körning zum Wilke-Preis für den besten Zweifach-Bachelor-Abschluss 2015 in Chemie.
 The annual meeting 2015 of the bio-N3MR network NRW was the first symposium of our network to be held at the Ruhr Universiy of Bochum. Junior scientists of the participating groups presented their current research projects at the symposium in lecture hall HNC10, followed by a poster session. After lunch, the participants of the bio-N3MR meeting joined the NMR session of the „European Conference on the Spectroscopy of Biological Molecules", which took place in parallel at Ruhr University of Bochum.
The annual meeting 2015 of the bio-N3MR network NRW was the first symposium of our network to be held at the Ruhr Universiy of Bochum. Junior scientists of the participating groups presented their current research projects at the symposium in lecture hall HNC10, followed by a poster session. After lunch, the participants of the bio-N3MR meeting joined the NMR session of the „European Conference on the Spectroscopy of Biological Molecules", which took place in parallel at Ruhr University of Bochum.
 Function and regeneration of switch proteins impaired
Bochum and Wuppertal-based researchers study effects on enzymes
Bisphenol A impairs the function of proteins that are vital for growth processes in cells. This finding has been reported by researchers from the Ruhr-Universität Bochum and the University of Wuppertal. The substance, short BPA, is contained in many plastic products and is suspected of being hazardous to health. To date, it had been assumed that bisphenol A produces a harmful effect by binding to hormone receptors. The chemist and biochemist team has discovered that the substance also affects the so-called small GTPases. They published their findings in the “Journal of Medicinal Chemistry”.
Function and regeneration of switch proteins impaired
Bochum and Wuppertal-based researchers study effects on enzymes
Bisphenol A impairs the function of proteins that are vital for growth processes in cells. This finding has been reported by researchers from the Ruhr-Universität Bochum and the University of Wuppertal. The substance, short BPA, is contained in many plastic products and is suspected of being hazardous to health. To date, it had been assumed that bisphenol A produces a harmful effect by binding to hormone receptors. The chemist and biochemist team has discovered that the substance also affects the so-called small GTPases. They published their findings in the “Journal of Medicinal Chemistry”.
 |
Wir gratulieren recht herzlich unserer Mitarbeiterin Miriam Schöpel zum GBM-Preis 2013 der "Gesellschaft für Biochemie und Molekularbiologie e.V." für die beste Masterarbeit im Studiengang Biochemie.
 RUB-Forscher entschlüsseln Zusammenspiel von Enkephalinen und Schmerzrezeptoren
Metallkomplex macht flüchtigen Botenstoff dingfest
„Schmerz lass nach!“ Um dieses Signal zu senden, produziert der menschliche Körper kleine Botenstoffmoleküle, die an bestimmte Rezeptoren andocken. Dieses Zusammenspiel zwischen den Botenstoffen, Enkephaline genannt, und Opioidrezeptoren ist mit herkömmlichen biochemischen Methoden schwer zu untersuchen. Einem interdisziplinären Team von Biochemikern und Anorganischen Chemikern der Ruhr-Universität Bochum (RUB) gelang es nun, die Struktur eines Enkephalins in Lösung zu bestimmen und erstmals seine Interaktion mit dem Opioidrezeptor im Detail zu verfolgen. Die Analyse liefert präzise neue Ansatzpunkte für die Entwicklung von Medikamenten, die gezielt bestimmte Arten von Schmerz bekämpfen. Die Zeitschrift „Dalton Transactions“ widmet dem Thema die Titelgeschichte.
RUB-Forscher entschlüsseln Zusammenspiel von Enkephalinen und Schmerzrezeptoren
Metallkomplex macht flüchtigen Botenstoff dingfest
„Schmerz lass nach!“ Um dieses Signal zu senden, produziert der menschliche Körper kleine Botenstoffmoleküle, die an bestimmte Rezeptoren andocken. Dieses Zusammenspiel zwischen den Botenstoffen, Enkephaline genannt, und Opioidrezeptoren ist mit herkömmlichen biochemischen Methoden schwer zu untersuchen. Einem interdisziplinären Team von Biochemikern und Anorganischen Chemikern der Ruhr-Universität Bochum (RUB) gelang es nun, die Struktur eines Enkephalins in Lösung zu bestimmen und erstmals seine Interaktion mit dem Opioidrezeptor im Detail zu verfolgen. Die Analyse liefert präzise neue Ansatzpunkte für die Entwicklung von Medikamenten, die gezielt bestimmte Arten von Schmerz bekämpfen. Die Zeitschrift „Dalton Transactions“ widmet dem Thema die Titelgeschichte.

Das Protein Ras in Lösung, an der Membran und in der Signaltrans-
duktionskaskade innerhalb der lebenden Zelle (von links nach rechts).
Die RUB, die TU Dortmund und das Dortmunder MPI freuen sich über die Verlängerung des Sonderforschungsbereichs 642 (Sprecher: Prof. Klaus Gerwert, RUB) um weitere 3,5 Jahre. Von der Struktur- bis zur Systembiologie, von der Biophysik über die chemische Biologie bis hin zur Zellbiologie arbeiten Wissenschaftler aus Bochum und Dortmund fachübergreifend in der Proteinforschung zusammen.
Mit der nun bewilligten weiteren Förderung von 7,2 Mio. Euro wurden über die volle Laufzeit von insgesamt zwölf Jahren rund 20,3 Mio. Euro eingeworben. Insgesamt sind 17 Projekte aus den Bochumer Fakultäten für Biologie, Chemie und Medizin sowie der Technischen Universität und dem Max Planck Institut für molekulare Physiologie in Dortmund am bereits 2004 gegründeten SFB 642 „GTP- und ATP-abhängige Membranprozesse“ beteiligt.
 Researchers at the RUB and from Berkeley have used metal complexes to modify peptide hormones. In the Journal of the American Chemical Society, they report for the first time on the three-dimensional structure of the resulting metal-peptide compounds. “With this work, we have laid the molecular foundation for the development of better medicines” says Prof. Raphael Stoll from the Faculty of Chemistry and Biochemistry at the Ruhr-University. The team examined hormones that influence the sensation of pain and tumour growth.
Researchers at the RUB and from Berkeley have used metal complexes to modify peptide hormones. In the Journal of the American Chemical Society, they report for the first time on the three-dimensional structure of the resulting metal-peptide compounds. “With this work, we have laid the molecular foundation for the development of better medicines” says Prof. Raphael Stoll from the Faculty of Chemistry and Biochemistry at the Ruhr-University. The team examined hormones that influence the sensation of pain and tumour growth.
 Einladung zur 34. GDCh-Diskussionstagung
Einladung zur 34. GDCh-Diskussionstagung
"Praktische Probleme der Kernresonanz-
spektroskopie"
14. - 15. Januar 2013 in Erlangen.
Die Teilnahme ist wie immer gebührenfrei.
 Mutierte Proteine ausschalten und so bösartige Tumore bekämpfen – das ist das Ziel des neuen Gemeinschaftsprojektes von Wuppertaler und Bochumer Forschern. Zu diesem Zweck kooperiert die RUB-Arbeitsgruppe Biomolekulare NMR-Spektroskopie von Prof. Dr. Raphael Stoll mit der Wuppertaler Arbeitsgruppe Bioorganische Chemie unter Leitung von Prof. Dr. Jürgen Scherkenbeck. Die Deutsche Krebshilfe fördert das Vorhaben zwei Jahre lang mit 200.000 Euro.
Mutierte Proteine ausschalten und so bösartige Tumore bekämpfen – das ist das Ziel des neuen Gemeinschaftsprojektes von Wuppertaler und Bochumer Forschern. Zu diesem Zweck kooperiert die RUB-Arbeitsgruppe Biomolekulare NMR-Spektroskopie von Prof. Dr. Raphael Stoll mit der Wuppertaler Arbeitsgruppe Bioorganische Chemie unter Leitung von Prof. Dr. Jürgen Scherkenbeck. Die Deutsche Krebshilfe fördert das Vorhaben zwei Jahre lang mit 200.000 Euro.
 Tag der offenen Tür im Alfried Krupp-Schülerlabor am 24.09.2011
Tag der offenen Tür im Alfried Krupp-Schülerlabor am 24.09.2011
Tag der offenen Tür für alle Neugierigen - Entdecken & Begreifen von MINT und Geisteswissenschaften
Am 24.09.2011 von 10.00 bis 15.00 Uhr öffnet das Schülerlabor seine Türen und heißt alle Neugierigen willkommen! Bei uns gilt: mitmachen - forschend lernen - an einem spannenden Ort auf kluge Weise experimentieren. Wir sind eines der vielfältigsten Schülerlabore in ganz Deutschland, und am Tag der offenen Tür zeigen wir Experimente und Materialien aus unseren Projekten zum Anfassen und selber Ausprobieren.
 Zwei junge Krebsforscher der Ruhr-Universität können sich über Unterstützung bei ihren Dissertationsprojekten freuen: King Tuo Yip (Biochemie, Betreuer: Prof. Dr. Raphael Stoll) und Swetlana Ladigan (Pathologie, Betreuer: Dr. Alireza Mirmohammadsadegh) wurden bei der diesjährigen FoRUM-Tagung der Medizinischen Fakultät der RUB mit den Stipendien der Schäfersnolte-Gedächtnis-Stiftung ausgezeichnet und erhalten für ein Jahr monatlich 1.200 Euro Förderung. Im Mittelpunkt ihrer Arbeiten stehen detaillierte Untersuchungen zur Entwicklung von Darmkrebs und zur Bildung von Metastasen beim schwarzen Hautkrebs.
Zwei junge Krebsforscher der Ruhr-Universität können sich über Unterstützung bei ihren Dissertationsprojekten freuen: King Tuo Yip (Biochemie, Betreuer: Prof. Dr. Raphael Stoll) und Swetlana Ladigan (Pathologie, Betreuer: Dr. Alireza Mirmohammadsadegh) wurden bei der diesjährigen FoRUM-Tagung der Medizinischen Fakultät der RUB mit den Stipendien der Schäfersnolte-Gedächtnis-Stiftung ausgezeichnet und erhalten für ein Jahr monatlich 1.200 Euro Förderung. Im Mittelpunkt ihrer Arbeiten stehen detaillierte Untersuchungen zur Entwicklung von Darmkrebs und zur Bildung von Metastasen beim schwarzen Hautkrebs.
 Das Signalprotein Rheb kommt in vielen Körperzellen, besonders im Gehirn vor. Es ist wichtig für Wachstumsprozesse – bei Zellstress zeigt es aber sein zweites Gesicht. In diesem Fall beschleunigt es den Tod der Zelle. Diese Erkenntnis haben Forscher um Prof. Dr. Rolf Heumann und Prof. Dr. Raphael Stoll von der Ruhr-Universität Bochum gewonnen.
Sie hat Auswirkungen auf die Behandlung von Erkrankungen: Das verbreitet eingesetzte Antibiotikum Rapamycin, das die Signalweiterleitung von Rheb verhindert, sollte mit Bedacht eingesetzt werden, raten die Forscher. Unter Zellstressbedingungen könnte sich seine Wirkung umkehren. Die Forscher berichten im Journal of Biological Chemistry.
Das Signalprotein Rheb kommt in vielen Körperzellen, besonders im Gehirn vor. Es ist wichtig für Wachstumsprozesse – bei Zellstress zeigt es aber sein zweites Gesicht. In diesem Fall beschleunigt es den Tod der Zelle. Diese Erkenntnis haben Forscher um Prof. Dr. Rolf Heumann und Prof. Dr. Raphael Stoll von der Ruhr-Universität Bochum gewonnen.
Sie hat Auswirkungen auf die Behandlung von Erkrankungen: Das verbreitet eingesetzte Antibiotikum Rapamycin, das die Signalweiterleitung von Rheb verhindert, sollte mit Bedacht eingesetzt werden, raten die Forscher. Unter Zellstressbedingungen könnte sich seine Wirkung umkehren. Die Forscher berichten im Journal of Biological Chemistry.
 Es geht erfolgreich weiter mit der Proteinforschung an der RUB: der SFB 642 (GTP und ATP abhängige Membranprozesse, Sprecher Klaus Gerwert) wird für weitere vier Jahre bis 2012 gefördert. Nach vier Jahren kooperativer Forschung von 2004-2008 ist der SFB bei der internationalen zweitätigen Begutachtung am 9./10. April in Bochum „als exzellentes, international sichtbareres Cluster“ bewertet und das Fördervolumen nach einer strengen Prüfung durch den Bewilligungsausschuss der DFG am 20. Mai von 6 auf 9,6 Millionen Euro aufstockt worden. Zusätzlich wurden 12 Doktoranden Stipendien für eine SFB interne Graduierten-Ausbildung zur Förderung des wissenschaftlichen Nachwuchses bewilligt.
Es geht erfolgreich weiter mit der Proteinforschung an der RUB: der SFB 642 (GTP und ATP abhängige Membranprozesse, Sprecher Klaus Gerwert) wird für weitere vier Jahre bis 2012 gefördert. Nach vier Jahren kooperativer Forschung von 2004-2008 ist der SFB bei der internationalen zweitätigen Begutachtung am 9./10. April in Bochum „als exzellentes, international sichtbareres Cluster“ bewertet und das Fördervolumen nach einer strengen Prüfung durch den Bewilligungsausschuss der DFG am 20. Mai von 6 auf 9,6 Millionen Euro aufstockt worden. Zusätzlich wurden 12 Doktoranden Stipendien für eine SFB interne Graduierten-Ausbildung zur Förderung des wissenschaftlichen Nachwuchses bewilligt.
 21.03.2007 - Ein Netzwerk für Biomolekulare Kernspintomographie (NMR) wurde mit Beteiligung des Forschungszentrums Jülich in Düsseldorf gegründet. Jülich verfügt neben seiner wissenschaftlichen Expertise über ein NMR-Zentrum mit drei leistungsstarken Spektrometern.
Das NRW-Netzwerk bio-N3MR wurde als eine Kooperation des Forschungszentrums Jülich, der Heinrich-Heine-Universität Düsseldorf, der Ruhr-Universität Bochum, der Universität Duisburg-Essen sowie dem Max-Planck-Institut für molekulare Physiologie in Dortmund im Bereich der NMR-basierten strukturbiologischen Forschung gegründet.
21.03.2007 - Ein Netzwerk für Biomolekulare Kernspintomographie (NMR) wurde mit Beteiligung des Forschungszentrums Jülich in Düsseldorf gegründet. Jülich verfügt neben seiner wissenschaftlichen Expertise über ein NMR-Zentrum mit drei leistungsstarken Spektrometern.
Das NRW-Netzwerk bio-N3MR wurde als eine Kooperation des Forschungszentrums Jülich, der Heinrich-Heine-Universität Düsseldorf, der Ruhr-Universität Bochum, der Universität Duisburg-Essen sowie dem Max-Planck-Institut für molekulare Physiologie in Dortmund im Bereich der NMR-basierten strukturbiologischen Forschung gegründet.
 Wir gratulieren recht herzlich unserem Mitarbeiter Gerd Kock zum Wilke-Preis 2007 des "Vereins zur Förderung der Chemie und Biochemie" an der Ruhr-Universität Bochum für den besten Abschluss im Studiengang Biochemie.
Wir gratulieren recht herzlich unserem Mitarbeiter Gerd Kock zum Wilke-Preis 2007 des "Vereins zur Förderung der Chemie und Biochemie" an der Ruhr-Universität Bochum für den besten Abschluss im Studiengang Biochemie.













